Streszczenie
Wielu lekarzy unika stosowania środków znieczulających ze względu na obawy dotyczące powikłań związanych z toksycznością. Pojęcie potencjalnej toksyczności pojawia się zawsze, kiedy mamy do czynienia z jakimkolwiek powikłaniem. Logiczna wydaje się więc tendencja do zmniejszenia podawanej ilości środka znieczulającego z jednoczesnym zachowaniem skuteczności. Ponadto lekarz, dla komfortu pacjenta, musi dostosować długość trwania znieczulenia do długości zabiegu.
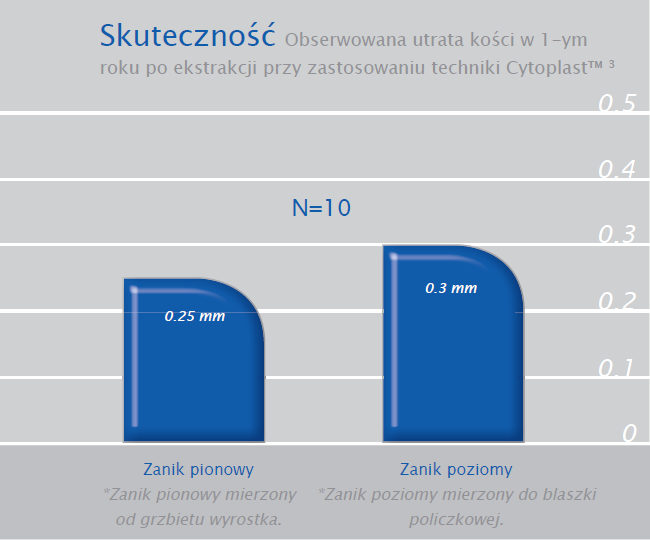
W trakcie opisywanego badania wykonano 500 znieczuleń dokostnych (transkortykalnych) zarówno w szczęce, jak i w żuchwie. Umożliwiło to czterokrotne ograniczenie podanych dawek przy zachowaniu identycznej skuteczności.
Dlaczego zmniejszać toksyczność anestetyku?
Jak podaje piśmiennictwo, „próg toksyczności u zdrowej osoby dorosłej o masie 72 kg zostaje osiągnięty po podaniu 13 ampułek o zawartości 1,8 ml 2% lidokainy bez środka obkurczającego naczynia i 8 ampułek z dodatkiem wazokonstryktora (1). Z kolei lekarz napotykający problem podczas wykonywania znieczulenia zawsze w pierwszej kolejności myśli o samym anestetyku jako jego przyczynie.
We wszystkich podręcznikach, pisząc o znieczuleniach, szczególny nacisk kładzie się na kwestię toksyczności produktów w przypadku dzieci, kobiet w ciąży, osób starszych lub też osób dotkniętych schorzeniami, które mogłyby zwiększyć toksyczność podanego produktu. Źródłem tego wzrostu toksyczności jest zmniejszenie normalnej zdolności pacjenta do metabolizowania produktu.
Dążymy więc do zmniejszenia toksyczności, również u pacjentów zdrowych (2), nie zapominając o podstawowej funkcji znieczulenia, czyli całkowitym wyeliminowaniu bólu podczas całe-go aktu zabiegowego. Ponadto zmniejszenie dawki anestetyku może pomóc w dokładnym dostosowaniu czasu działa-ia znieczulenia do długości zabiegu.
Nie jest naszym celem, tak jak to czynią podręczniki mówiące o znieczuleniach, omawianie poszczególnych patologii i opracowanie odpowiedniego sposobu postępowania, tylko określenie zasad, które umożliwią zmniejszenie toksyczności środka w większości przypadków.
Tym samym lekarz, pamiętając, iż tylko wyjątkowo będzie można brać pod uwagę toksyczność produktu, w razie wystąpienia problemów będzie musiał się zainteresować sposobami wykonania znieczulenia (3).
Jak zmniejszyć toksyczność znieczulenia?
Do zagadnienia toksyczności można podejść dwojako: w aspekcie jakościowym i ilościowym.
Roztwór anestetyku, jakikolwiek by był, zawsze składa się z 3 składowych: molekuły anestetyku (aminoamidy lub aminoestry), środka konserwującego i przeciwutleniacza (EDTA). Składowe te są potencjalnie toksyczne (4, 5) podobnie jak sama molekuła anestetyku. Jest to toksyczność jakościowa. Do tego podstawowego składu może być lub nie dodany środek obkurczający naczynia. Wazokonstryktor (adrenalina lub noradrenalina) jest endogenną katecholaminą, tak więc nie ma toksyczności farmakologicznej sensu stricte.
Nie wnikając w szczegóły porównań toksyczności poszczególnych anestetyków, należy jedynie odnotować, iż bupi-wakaina czy markaina odznaczają się wyższą kardiotoksycznością od pozostałych molekuł, ale warto pamiętać, iż są rzadko stosowane (4). Pominiemy również roztwory anestetyków pozbawione środków zwężających naczynia, ponieważ powinny być one stosowane wyjątkowo. Jeżeli chodzi o środki znieczulające z wazokonstryktorem, to roztwór lidokainy występuje w stężeniu 2%, podczas gdy roztwór artykainy w stężeniu 4%. Wydaje się więc oczywiste, iż przy podaniu identycznych ilości tych anestetyków (5, 6), to roztwór lidokainy jest dwukrotnie mniej toksyczny.
Aby uzyskać regularne zmniejszenie toksyczności ilościowej trzech składowych niebiologicznych, wystarczy zmniejszyć stężenie anestetyku oraz podawaną ilość.
Standardowo stosowane ilości
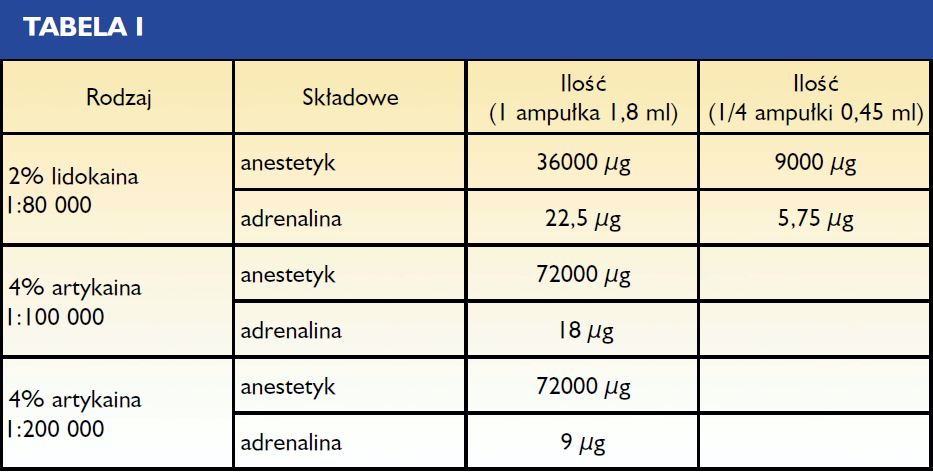
Porównanie różnych podręczników poruszających zagadnienie znieczuleń pokazuje, iż nieliczne są przypadki określenia precyzyjnych ilości. Jedynie Hans Evers podaje dokładne dane ilościowe dla poszczególnych technik znieczuleń. Wszyscy autorzy natomiast zgodnie zauważają indywidualną zmienność osobniczą co do zasięgu, czasu trwania i głębokości znieczulenia przy podaniu tej samej ilości. Reasumując, można stwierdzić, iż w szczęce, przy znieczuleniu okołowierzchołkowym, podanym od strony przedsionkowej i podniebiennej z reguły zużywa się ampułkę anestetyku (7, 8). W żuchwie, w odcinku przednim oraz okolicy przedtrzonowców również podaje się ampułkę znieczulenia od strony przedsionkowej uzupełnioną iniekcją od strony językowej. Jeżeli chodzi o znieczulenie przewodowe, jako minimum należy traktować podanie 1 ampułki. Najczęściej zalecanym anestetykiem jest artykaina z dodatkiem adrenaliny w stężeniu 1:200 000 (ampułka 1,8 ml), co odpowiada 9 µg adrenaliny i 72 000 µg artykainy (5) (tab. I).
Jak zachować skuteczność znieczulenia, zmniejszając podawaną dawkę?
Przegląd piśmiennictwa pokazuje, iż jedynym sposobem zwiększenia skuteczności znieczulenia jest zwiększenie stężenia środka zwężającego naczynia (2, 6). Wiadomo, iż wazokonstryktor działa
na 2 poziomach:
• Ogólnym – zmniejszając toksyczność przez spowolnienie dyfuzji toksycznych molekuł w organizmie. Obniża natychmiastowe stężenie osoczowe (4, 5, 6). Wywołuje przejściową tachykardię bez jakichkolwiek konsekwencji ogólnoustrojowych (9).
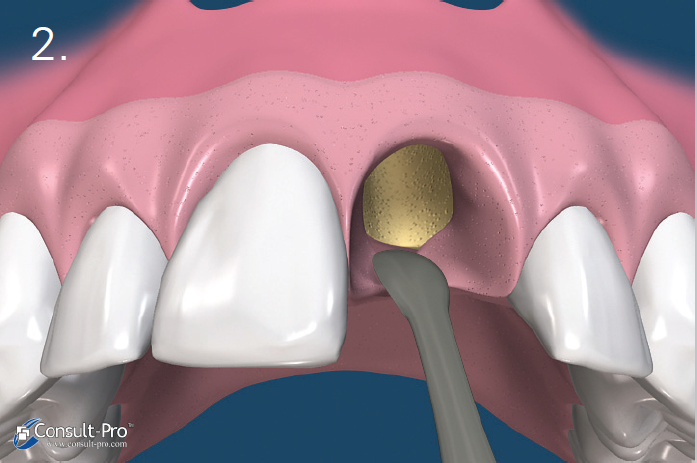
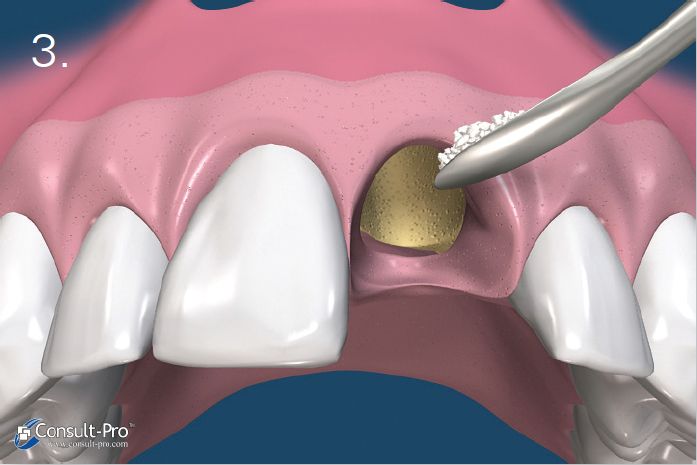
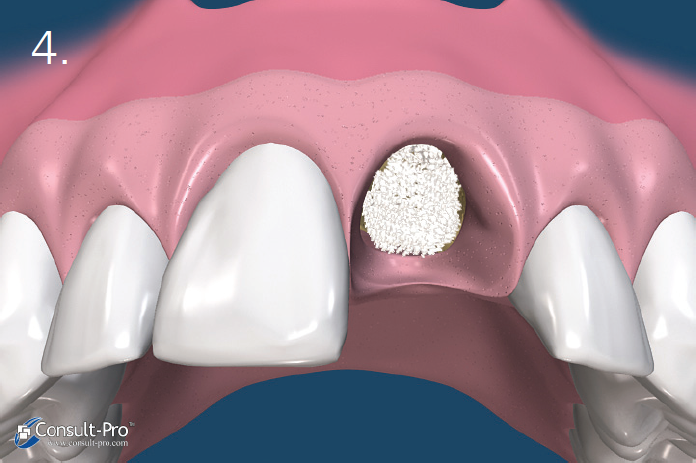
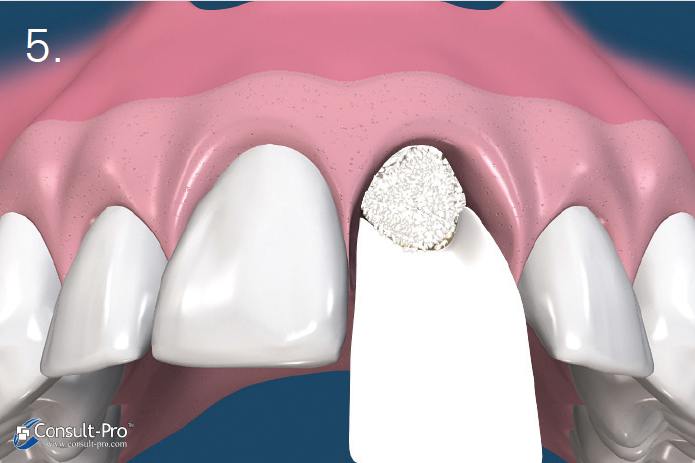
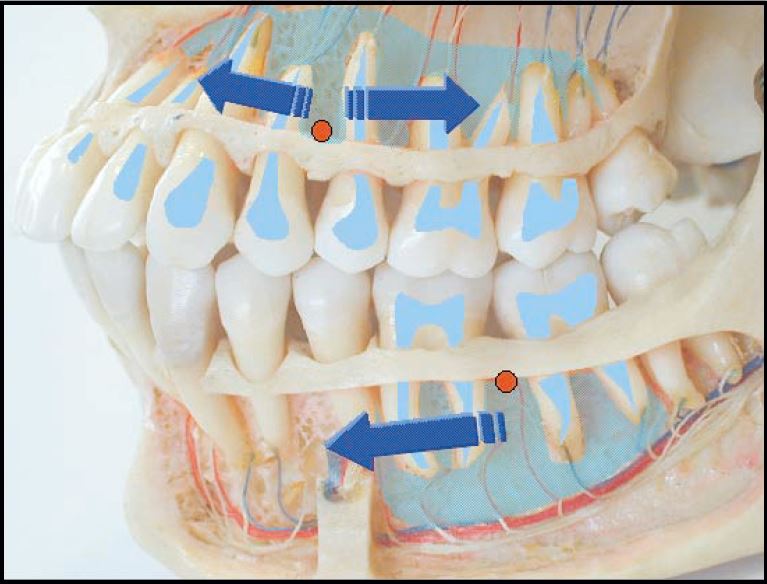
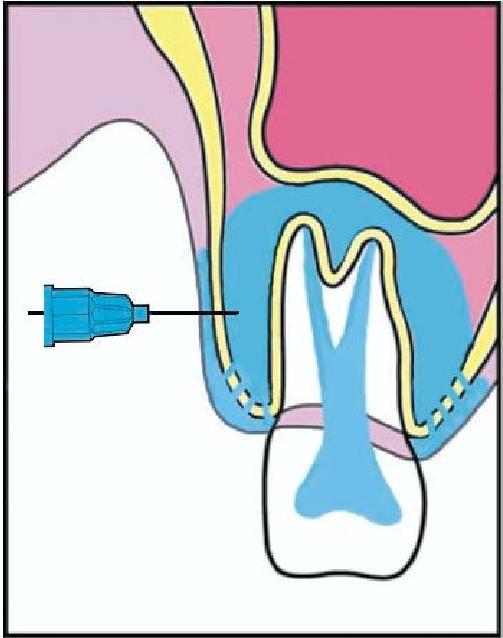
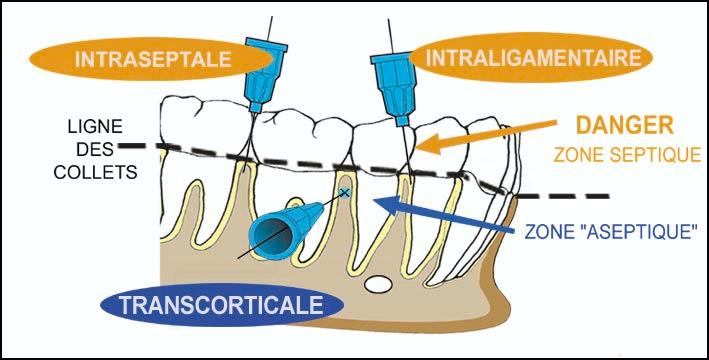
• Miejscowym – zwiększa skuteczność anestetyku (2, 6),wywołując mniejsze lub większe zwolnienie krążenia krwi. To niedokrwienie może wywołać efekty w stosunku do danej tkanki, proporcjonalne do jego zasięgu i czasu trwania. Efekt niedokrwienia będzie tym wyraźniejszy i bardziej przedłużony, im tkanka będzie słabiej ukrwiona. Niemożliwe i niebezpieczne jest więc istotne zwiększenie stężenia wazokonstryktora podczas wykonywania znieczuleń śródwięzadłowych, do przegrodowych czy dopodniebiennych, albowiem wiązałoby się to z niebezpieczeństwem martwicy tkanek (2). Jedynie tkanki obficie unaczynione umożliwiają stosowanie anestetyku z dodatkiem wazokonstryktora o dużym stężeniu bez ryzyka martwicy. Z histologicznego punktu widzenia tkanką najlepiej unaczynioną jest kość gąbczasta zlokalizowana pomiędzy zębodołami. Dlatego też właśnie do niej będzie można podać anestetyk z najwyższym stężeniem wazokonstryktora.
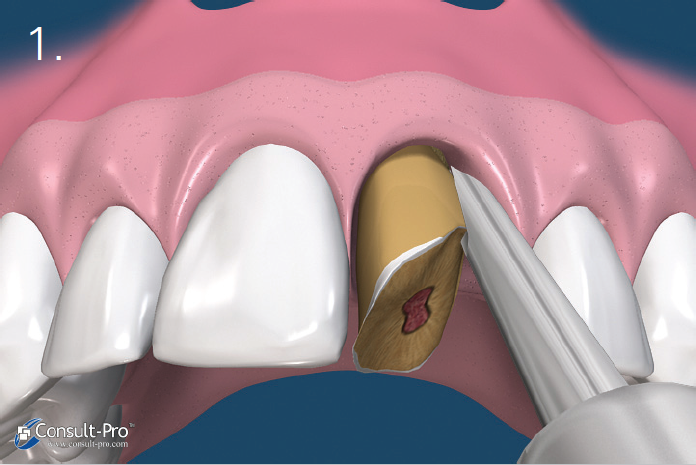
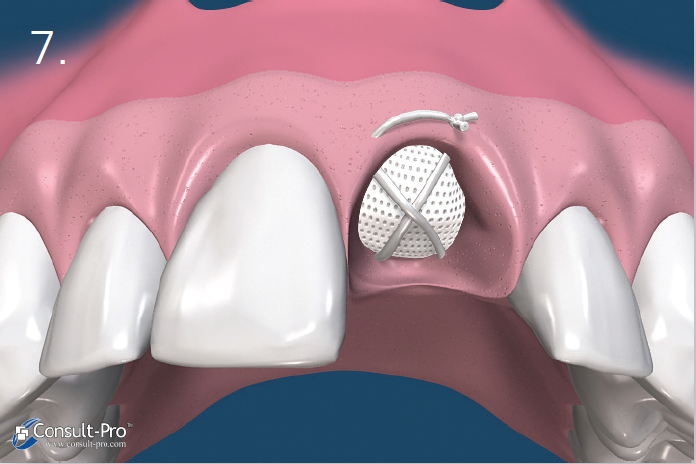
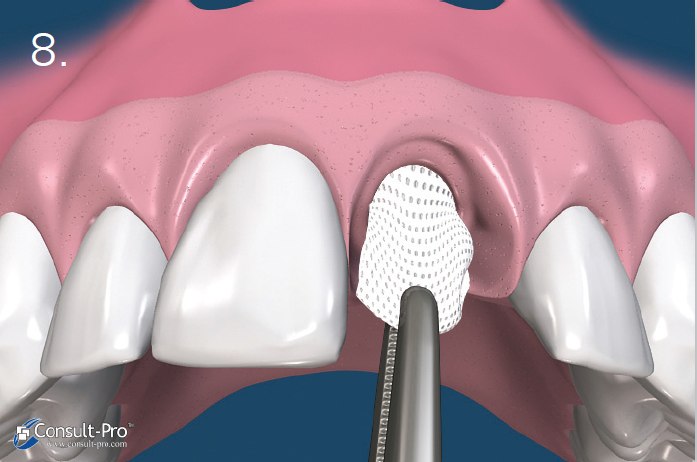
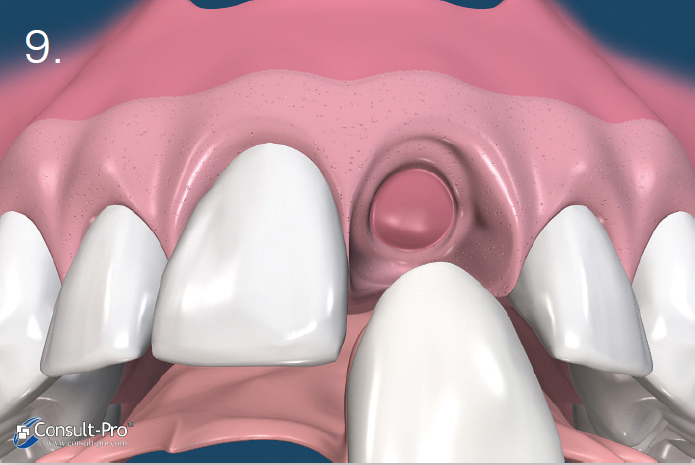
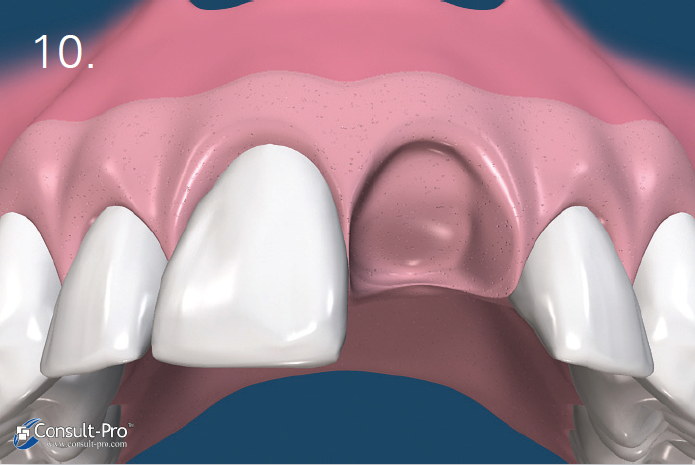
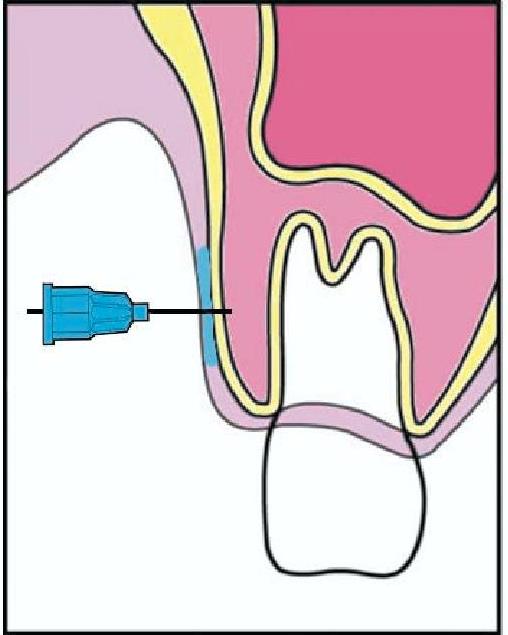
Tak więc znieczulenie dokostne (transkortykalne) w połączeniu z podaniem środka z wysokim stężeniem wazokonstryktora powinno stanowić rozwiązanie zadanego problemu.
Cechy badania
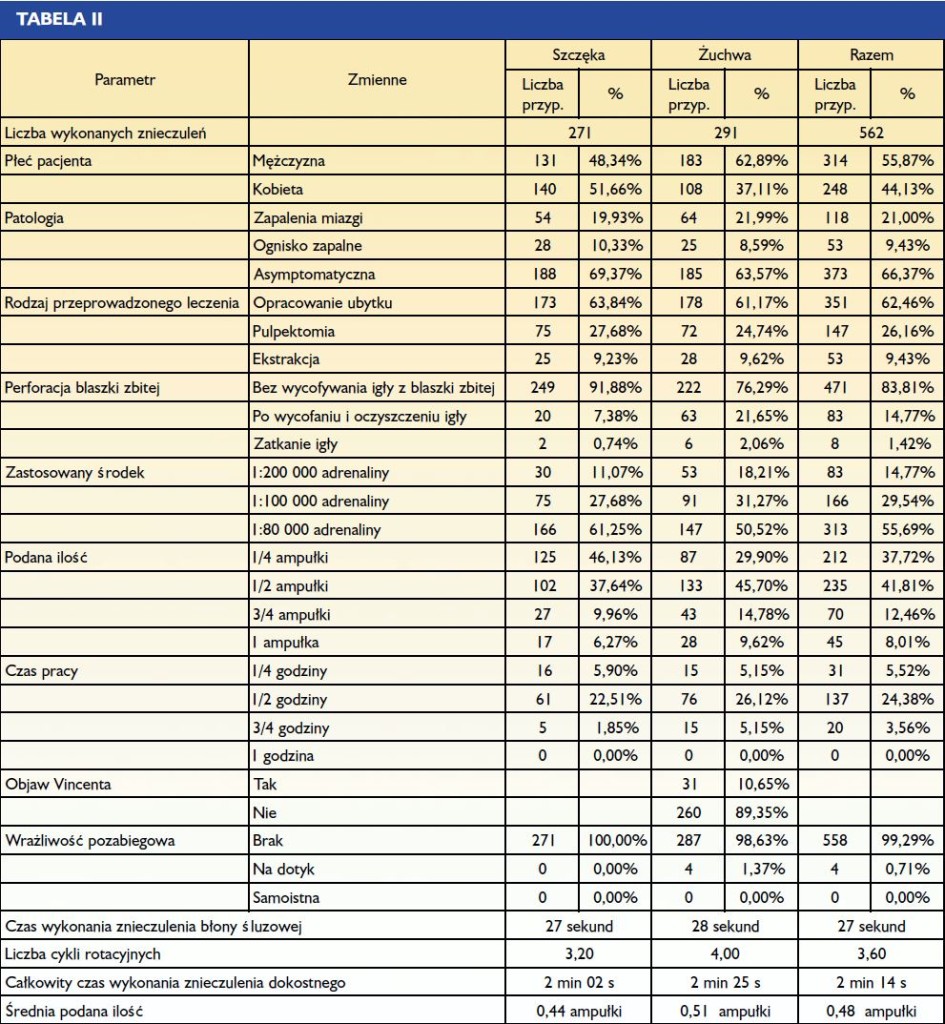
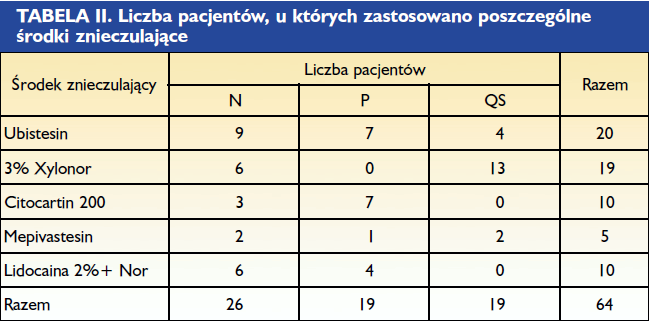
Badanie przeprowadzone w ramach prywatnej praktyki ogólnostomatologicznej polegało na wykonywaniu znieczuleń dokostnych zarówno w szczęce, jak i żuchwie, z zastosowaniem najczęściej jak było możliwe – w zależności od przypadku klinicznego – środka znieczulającego o stężeniu adrenaliny 1:80 000 przy podaniu 1/4 ampułki. Zanotowano cechy charakterystyczne każdego wykonanego znieczulenia, które zostały zawarte w tabeli II.
Środki
Środki znieczulające:
- Primakaina (roztwór 4% artykainy z dodatkiem adrenaliny w stężeniu 1:200 000 lub 1:100 000, laboratoires Pierre Rolland)
- Xylorolland (roztwór 2% lidokainy z dodatkiem 1:80 000 adrenaliny, laboratoires Pierre Rolland)
Igły:
- Transcort (C 0,40 mm, długość 12 mm, firma Dental Hi Tec)
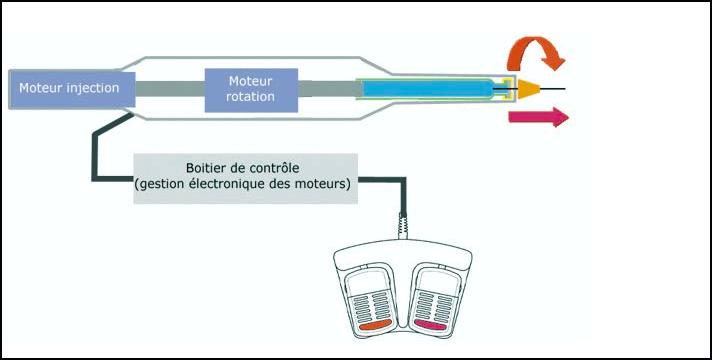
Urządzenie do perforacji i iniekcji:
- QuickSleeper (firma Dental Hi Tec)
Analiza zastosowanych produktów
Stwierdzono, iż znieczulenie dokostne z dodatkiem środka zwężającego naczynia wywołuje tachykardię (2, 4, 5, 7, 8, 10). Jest ona osobniczo zmienna i zależna również od ilości podanego
wazokonstryktora. Analiza treści tabeli I pokazuje, iż ilość adrenaliny zawarta w 1/4 ampułki lidokainy (stężenie 1:80 000 środka zwężającego) jest prawie o połowę mniejsza od ilości zawartej w całej 1 ampułce (stężenie 1:200 000), która jest standardowo stosowana do znieczuleń okołowierzchołkowych. Jeżeli natomiast chodzi o ilość samego anestetyku, w 1/4 ampułki lidokainy
(1:80 000) jest ona osiem razy mniejsza niż w 1 ampułce artykainy (1:200 000 lub 1:100 000) (tab. I). Lidokainę i artykainę cechuje taka sama toksyczność (6, 11), jak i skuteczność (5, 12).
Z analizy tej wynika, iż dokostne podanie 1/4 ampułki lidokainy (1:80 000) umożliwia uzyskanie ośmiokrotnie niższej toksyczności niż okołowierzchołkowe podanie 1 ampułki artykainy (1:200 000) (tab. I).
Analiza wyników
Nie zróżnicowaliśmy przypadków klinicznych, w których zastosowano lidokainę (1:80 000). Stanowią one 55% ogółu. W przypadkach leczenia jednego lub dwóch zębów podawano 1/4 ampułki
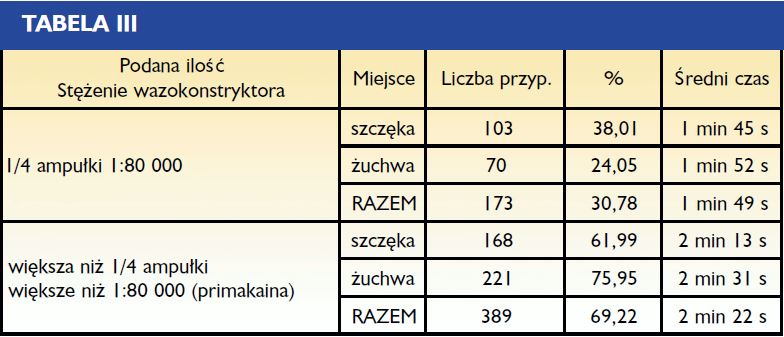
(1:80 000). Pozostałe przypadki kliniczne (skaling, leczenie obejmujące całe łuki lub odcinek od kła od kła) wymagały podania większej ilości primakainy (1:200 000 lub 1:100 000). Przypadki, w których wykorzystano 1/4 ampułki (1:80 000) poddano szczegółowej analizie w tabeli III.
Dyskusja
Analiza tabeli II pokazuje, że:
- Ogólnie dokonano 562 znieczuleń, z których 55,69% miało dodatek wazokonstrykotora o stężeniu 1:80 000, bez wystąpienia żadnej reakcji martwiczej tkanki.
- Średni czas wykonania znieczulenia dokostnego w opisywanym badaniu był krótszy niż w pierwszym badaniu i wyniósł 2 minuty 14 sekund (w pierwszym badaniu 2 min 38 s) (12).
- Znieczulenia wykonane z użyciem 1/4 ampułki trwały 1 minutę 5 sekund w żuchwie i 1 minutę 42 sekundy w szczęce. Średnia wyniosła 1 min 49 s, co jest czasem bardzo krótkim (tab. III).
- Średnia podana ilość anestetyku spadła do 0,48 ampułki bez względu na patologię i liczbę znieczulonych zębów.
Wnioski
Znieczulenie dokostne umożliwia iniekcję lidokainy w stężeniu 1:80 000. Podanie 1/4 ampułki jest szybkie i umożliwia natychmiastowe znieczule-nie dwóch sąsiadujących zębów w obrębie żuchwy i szczęki. Taka iniekcja powoduje głębokie znieczulenie danych zębów z toksyczno-ścią ośmiokrotnie mniejszą niż podczas znieczulenia okołowierzchołkowego. Wzrost stężenia wazokonstryktora umożliwia zwiększenie skuteczności znieczulenia (stany zapalne miazgi, ogniska zapalne). Zmniejszenie ilości pociąga za sobą zmniejszenie toksyczności i kompensuje wzrost stężenia wazokonstryktora.
Wzrost stężenia środka zwężającego naczynia i zmniejszenie podawanych ilości środka znieczulającego związane z wykonywaniem znieczulenia dokostnego umożliwiają uzyskanie znieczulenia skuteczniejszego, zgodnego w czasie i lepiej dostosowanego do aktu zabiegowego, gwarantując jednocześnie maksymalny komfort pacjentowi.
Autor: Alain Villette, D.C.D., D.S.O, C.E.S. w dziedzinie biologii jamy ustnej, periodontologii i protetyki Przewodniczący l’Association Francaise pour le Perfectionnement en Anesthesie Dentaire, Praktyka Prywatna, Nantes
Przekład: lek. stom. Piotr Kaczmarek, Association de Recherche en Odontologie et Chirurgie Maxillo-Faciale, Paryż
Pierwotnie opublikowano w: Magazyn Stomatologiczny, 2004, 11, str. 14-17